自然指考分科
110指考化學考科-22
110指考化學考科-23
乙醇為一種生質燃料,可由葡萄糖經生物發酵作用生成。葡萄糖可從光合作用產生,以澱粉或纖維素形式儲存。葡萄糖發酵時除產生乙醇外,也同時生成產物甲。已知相關分子的真耳生成熱分別為二氧化碳:-393.5、乙醇:-277.7、葡萄糖:-1260、水:-285.8(kJ/mol)。
下列相關的敘述,哪些選項正確?
(A) 產物甲為水
(B) 葡萄糖發酵生成乙醇為放熱反應
(C) 從澱粉及纖維素產生葡萄糖,均需經過水解
(D) 葡萄糖經過發酵,所產生的乙醇與產物甲,兩者真耳數相同
(E) 葡萄糖發酵取得的乙醇,其燃燒的反應熱,比直接將原本的葡萄糖燃燒所產生的熱量多
110指考化學考科-24
去年(2020)諾貝爾化學獎頒發給兩位女性科學家,分別是艾曼紐爾·夏本提爾與珍妮佛·道納。她們發現了 CRISPR/Cas9 基因剪刀的技術,可以精準地剪接去氧核糖核酸(DNA)。這種技術可用於各種生物科技上,例如育種、醫藥和治療上。下列有關 DNA 的敘述,哪些正確?
(A) DNA之立體結構為雙股螺旋
(B) DNA與RNA分子具有4種相同的含氮鹼基
(C) DNA是以核苷酸為單體所聚合而成的巨大分子
(D) DNA分子中的核糖含有六個碳原子
(E) DNA分子鹼基間的氫鍵作用力,是其形成立體結構的重要因素之一
110指考化學考科-25
一、張老師與學生討論有關解題時的推理及類比思維方法後,給了學生一個有關物質的質量、原子量、分子量以及莫耳數的題目。
室溫時,某混合氣體G,無色無味無毒,是由兩種氣體X與Y等莫耳數混合而成,且G中X與Y的質量比為7:8。其中,液態X可作為儲存疫苗的冷劑;某些新冠肺炎的患者,藉由高壓Y氣體以維持生命。
然後張老師再給了一道新題目:在80℃時,混合氣體R是無色,也是由兩種氣體P與Q等莫耳數混合而成,R中P與Q的質量比也是7:8,但是兩者皆為有毒氣體,而且降低到室溫後,其中之一會變成液體。另外,氣體P是瓦斯燃燒不完全時,容易產生的氣體;氣體Q則為醇類。
根據這些敘述,回答下列問題:
1. 寫出X與Y的分子式。
2. 寫出P與Q的分子式。
110指考化學考科-26
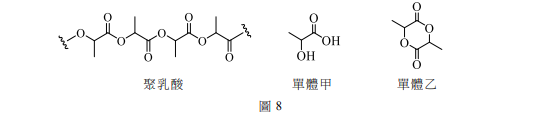
二、取12.0mg的某一含碳、氫、氧的化合物甲,經完全燃燒後,得26.4mg的CO₂及14.4mg的H₂O。另取12.0g的甲,在1.0L的容器加熱,當完全氧化時,測得容器的溫度為127℃,壓力為6.56atm。
根據這些實驗結果,回答下列問題:
1. 寫出化合物甲的實驗式。
2. 寫出化合物甲的分子量。
3. 寫出化合物甲的分子式,並畫出化合物甲之所有可能的結構異構物。
110指考化學考科-27
三、丹麥今年啟動了氮氣工業生產的綠色程序,使用固態氣離子電解槽(SOEC),過程中不需要高成本的空氣分離,圖9為其裝置示意圖。將適當比例的空氣和水蒸氣通入陰極,兩者均進行電解,氧氣生成O²⁻,水蒸氣產生H₂和O²⁻。氣離子薄膜只允許氧離子(O²⁻)通過,並在陽極反應。已知SOEC電解水的效率可達80%,在通入莫耳數比為1:3的空氣和水蒸氣後,經電解生成甲和乙兩部分的氣體。甲含有未反應的水蒸氣,將甲通過除水裝置後,直接導入哈柏法製程,即可製造氨。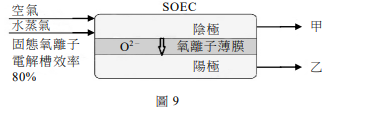
根據這些實驗結果,回答下列問題:
1. 寫出甲部分的氣體中,除了水蒸氣外,所含兩種主要氣體的化學式。
2. 寫出兩種在實驗室中用於吸收水蒸氣的常用化合物的化學式。
3. 寫出陽極的係數平衡電化學半反應式。
4. 已知SOEC電解水的效率可達80%。由化學計量的觀點,說明在此效率下,需要通入莫耳數比為1:3的空氣和水蒸氣的原因。
111分科化學考科-01
[題組:第1題]
已知氣氣與氯化氫反應後,可生成固體的產物,其反應式如下:
\[ \text{NH}_3 (\text{g}) + \text{HCl} (\text{g}) \rightarrow \text{NH}_4 \text{Cl} (\text{s}) \]
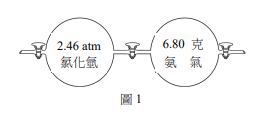
假設有一裝置容器,左、右各是2.00升的球體,中間有一個氣體閥門(如圖1)。在27℃,先將中間的氣體閥門關起來,左右邊球體內裝入6.80克的氣氣,在左邊球體裝入2.46 atm的氯化氫氣體。置入氣體後,將左、右氣體閥門關閉,再將中間氣體閥門打開,使左、右氣體完全混合且反應完全。假設氣氣和氯化氫氣體皆為理想氣體,且反應前後溫度不變,生成的固體體積可忽略。上述實驗後,容器內所剩的氣體與其壓力為何?
(A) 1.23 atm的氣氣
(B) 2.46 atm的氣氣
(C) 3.69 atm的氣氣
(D) 1.23 atm的氯化氫
(E) 2.46 atm的氯化氫
111分科化學考科-02
在溫度 1000 K 下,已知反應式 \( 2\text{N}_2\text{O(g)} \rightarrow 2\text{N}_2\text{(g)} + \text{O}_2\text{(g)} \),其反應速率常數為 0.76 s\(^{-1}\)。在此溫度下,若將 1.0 莫耳 N\(_2\)O(g) 注入 5.0 公升的真空容器內,則 N\(_2\)O 的初始反應速率是多少 (M/s)?
(A) \( 7.60 \times 10^{-1} \)
(B) \( 1.52 \times 10^{-1} \)
(C) \( 3.04 \times 10^{-2} \)
(D) \( 6.08 \times 10^{-2} \)
(E) \( 6.08 \times 10^{-3} \)
111分科化學考科-03
[題組:第3-4題]
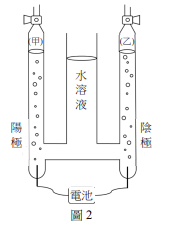
實驗課時進行電解濃食鹽水的實驗,實驗設計是以碳棒做為電極。大部分的學生實驗結果如圖 2 所示,陰極與陽極皆會產生氣體,且甲管與乙管的液面高度大致相同。
表1
| 半反應式 | E° (V) |
|---|---|
| \(\text{O}_2\text{(g)} + 4\text{H}^+ + 4\text{e}^- \rightarrow 2\text{H}_2\text{O}\) | 1.229 |
| \(\text{SO}_4^{2-} + \text{H}_2\text{O} + 2\text{e}^- \rightarrow \text{SO}_3^{2-} + 2\text{OH}^-\) | -0.936 |
| \(\text{NO}_3^-(\text{aq}) + 2\text{H}^+ + \text{e}^- \rightarrow \text{NO}_2\text{(g)} + \text{H}_2\text{O}\) | 0.80 |
| \(\text{Cl}_2\text{(g)} + 2\text{e}^- \rightarrow 2\text{Cl}^-\) | 1.36 |
| \(\text{Ag}^+(\text{aq}) + \text{e}^- \rightarrow \text{Ag(s)}\) | 0.80 |
但是,有五組的學生誤將其他鹽類當成食鹽配成水溶液進行電解實驗。誤拿的五種鹽類,事後發現應為亞硫酸鈉、硝酸銀、氯化鉀、硫酸鎂、硝酸銅。學生找資料查到可能相關的標準還原電位數據,如表 1 所示。根據以上結果,回答下列問題。
3 在大部分學生正確使用濃食鹽水的結果中,甲管的氣體應為下列何者?
(A)氫氣
(B)氧氣
(C)氮氣
(D)氯氣
(E)二氧化碳