112分科化學
112分科化學考科-12
鉀與氯氣反應形成氯化鉀,其他學反應式和反應熱如式 2 所示:
\[ K(s) + \frac{1}{2} Cl_2(g) \rightarrow KCl(s) \quad \Delta H^0 = -437 \, kJ/mol \quad (\text{式 2}) \]
表 1 是相關過程的能量變化(\(\Delta H^0\)):
| 過程 | \(\Delta H^0\) (kJ/mol) |
|---|---|
| K(s) → K(g) | 甲 |
| K(g) → K⁺(g) + e⁻ | 乙 |
| Cl₂(g) → 2 Cl(g) | 丙 |
| Cl(g) + e⁻ → Cl⁻(g) | 丁 |
| K⁺(g) + Cl⁻(g) → KCl(s) | 戊 |
根據以上資料,試問下列敘述,哪些正確?
(A) 甲 + 乙 + 丙 + 丁 + 戊 = -437 kJ/mol
(B) 甲 > 0
(C) 乙 > 0
(D) 丙 > 0
(E) 以相同質量的鉀與氯氣完全反應產生氯化鉀,則氯為限量試劑
112分科化學考科-13
[題組:第13-14題]
未知的四類有機化合物A、B、C、D各為飽和直鏈的醇、烷、醛與羧酸的其中一種。圖3為其含不同碳數的此四類化合物沸點分布,其中,A1表示A系列含1個碳的化合物,A2表示A系列含2個碳的化合物,依此類推。由圖3可知各類化合物沸點高低順序。
13 下列關於此四類有機化合物的敘述,哪些正確?
(A)A1與B1為同系物
(B)A1、B1、C1、D1四種化合物在氣態時,以A1較接近理想氣體
(C)四種化合物中,只有D類化合物具有分子間的氫鍵
(D)常溫時,B1與D1可與金屬鈉反應產生氫氣
(E)C1可與多命試劑作用產生銀鎚
112分科化學考科-15
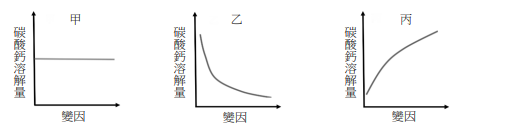
碳酸鈣固體溶於水為一放熱反應。下列甲、乙、丙三種圖形分別代表碳酸鈣固體在水中溶解量與施加變因的關係圖。下列相關變因的敘述,哪些正確?
(A)通入二氧化碳氣體,應為關係圖乙
(B)添加硝酸,應為關係圖丙
(C)添加硝酸鉀,應為關係圖乙
(D)添加碳酸鉀,應為關係圖乙
(E)升高溫度,應為關係圖甲
112分科化學考科-16
[題組:第16-17題]
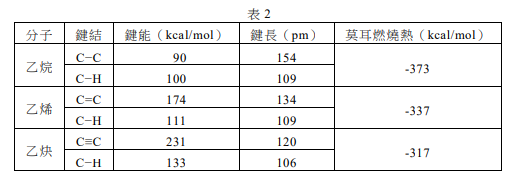
表2 比較乙烷、乙烯、乙炔三者的莫耳燃燒熱和碳-碳鍵、碳-氫鍵的鍵能和鍵長。
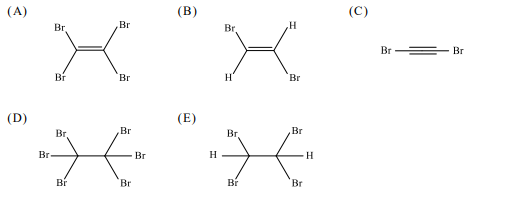
16 根據表2,下列關於乙烷、乙烯、乙炔三者的敘述哪些正確?
(A)將三種氣體完全燃燒後,若以生成每莫耳產物平均釋出的熱量來計算,最大者為乙炔
(B)將三種氣體各一莫耳完全燃燒後,總共放熱為1027卡
(C)碳-氫鍵的鍵長與鍵能間具有線性關係
(D)碳-碳鍵長越短,要打斷碳-碳鍵所需的能量越高
(E)打斷碳-碳參鍵所需能量是打斷碳-碳單鍵所需能量的三倍
112分科化學考科-18
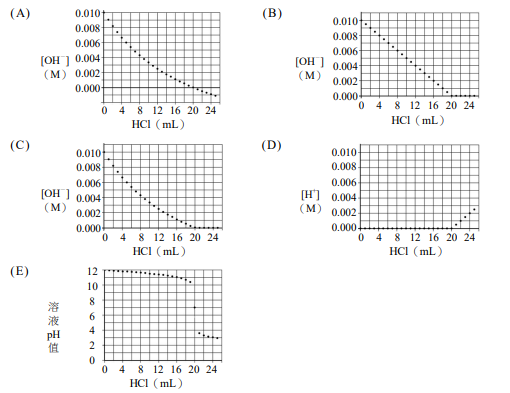
學生小軒將500毫升0.100M的氯化鉀以及500毫升0.100M的碘化鈉兩種溶液,依序加入0.100M的硝酸銀溶液1000毫升中,看見溶液出現白色沉澱與黃色沉澱。假設實驗前後,溶液的pH值均維持為7.0,且碘化銀與氯化銀的溶度積分別為 \( K_{sp(AgI)} \) 與 \( K_{sp(AgCl)} \),其中 \( K_{sp(AgI)} < K_{sp(AgCl)} \)。若達溶解度平衡時,下列關係式,哪些正確?
(A) \[ [Na^+] = [I^-] \]
(B) \[ [I^-] = [Cl^-] \]
(C) \[ [NO_3^-] = [Na^+] + [K^+] \]
(D) \[ [Ag^+] = (K_{sp(AgI)} + K_{sp(AgCl)})^{1/2} \]
(E) \[ [Ag^+] = (K_{sp(AgI)} \times K_{sp(AgCl)})^{1/2} \]
112分科化學考科-19
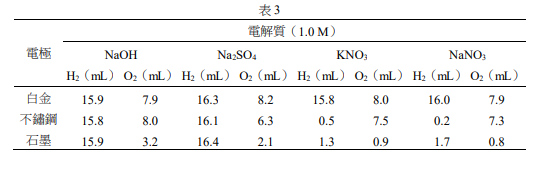
二次電池與我們的日常生活息息相關,鋰離子電池便是一例。近年來科學家開始發展一種同時具備金屬離子電池與燃料電池優點的二次電池,以鉑-空氣電池(圖4)為例,放電時電極反應如式3和式4所示:
\[ Zn + 2OH^- \rightarrow ZnO + H_2O + 2e^- \quad (\text{式3}) \]
\[ O_2 + 4H^+ + 4e^- \rightarrow 2H_2O \quad (\text{式4}) \]
下列關於鉑-空氣電池的敘述,哪些正確?
(A)在放電過程中,金屬鉑為陰極
(B)在放電過程中,陰極的產物為水
(C)此電池的全反應為 \( 2Zn + O_2 \rightarrow 2ZnO \)
(D)若將此電池的金屬鉑換成鎂,則無法進行放電反應
(E)若需對此電池進行充電,在充電過程中,水會氧化產生氧氣
112分科化學考科-20
[題組:第20-22題]
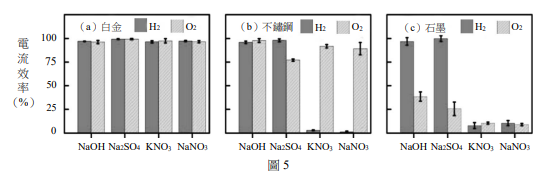
水電解反應所產生的氫氣(H2)與氧氣(O2),可分別作為燃料與醫療用途。為了瞭解電解質與電極材料對於水電解反應的影響,小安利用NaOH、Na2SO4、KNO3 與NaNO3 作為電解質,搭配白金、不鏽鋼與石墨作為電極,設計了一系列水電解實驗,並將結果整理成表3 與圖5;表3 為水電解實驗氣體生成體積,圖5 為水電解實驗的電流效率。電流效率表示所流通的電流中,有多少比例實際進行水電解反應。
20 下列關於實驗結果的敘述,哪些正確?(多選)
(A) 當使用白金電極時,氫氣或是氧氣的產量,並不隨電解質的不同而有明顯變化
(B) 當使用不鏽鋼電極時,無論電解質種類為何,氫氣都是主要產物
(C) 當使用石墨電極時,無論電解質種類為何,氫氣的產量都相同
(D) 若使用NaOH 或Na2SO4 當作電解質,無論電極材料為何,產氫的電流效率都接近100%
(E) 若使用KNO3 或NaNO3 當作電解質,不鏽鋼電極產氫和產氧的效率都比石墨電極佳