「大象牙膏」是一有趣的化學實驗:將濃度為30~35%的雙氧水與清潔劑混合,雙氧水分解產生的氧氣被清潔劑水溶液包裹住產生氣泡,此泡沫狀物質會像噴泉一樣噴湧而出。已知其化學反應式為:
\[ 2H_2O_2(l) \rightarrow 2H_2O(l) + O_2(g) \quad \Delta H^1 = -196 \, \text{kJ/mol} \]
活化能 \( E_a^1 = 76 \, \text{kJ/mol} \)。
若在此溶液中加入少量碘化鉀溶液,則泡沫噴湧的效果會更明顯。小安量測加入碘化鉀溶液後的反應活化能 \( E_a^2 = 57 \, \text{kJ/mol} \) 與反應熱 \(\Delta H^2 = -Q \, \text{kJ/mol} \)。此外,小安發現加入碘化鉀溶液後,碘離子會參與反應,而且有甲、乙兩反應發生。
甲:\( H_2O_2(l) + I^- (aq) \rightarrow Y(aq) + H_2O(l) \)
乙:\( H_2O_2(l) + Y(aq) \rightarrow Z(aq) + H_2O(l) + O_2(g) \)
已知甲、乙兩個反應的反應係數皆已平衡,且甲反應的反應速率小於乙反應的反應速率,小安分析反應後碘離子的量沒有減少。根據以上實驗觀察及結論,下列敘述哪些正確?
(A) \( Q > 196 \)
(B) \( Y \) 是 \( IO_3^- \)
(C) \( Z \) 是 \( I^- \)
(D) 甲反應活化能小於乙反應活化能
(E) 雙氧水在此實驗中既是氧化劑,也是還原劑
反應速率影響因素
112分科化學考科-08
利用柳酸與乙酐進行酯化反應,以少量濃硫酸作為催化劑,則可得到乙醯柳酸,乙醯柳酸又稱為阿司匹靈。實驗步驟如下:
(1) 在乾燥的10 mL試管內裝入2.0 mL乙酐。
(2) 秤取約1.00克的柳酸,倒入試管中。
(3) 試管中滴入3~5滴的濃硫酸,使柳酸完全溶解,混合均勻。
(4) 將試管置於70℃的熱水浴中15~20分鐘。
(5) 將試管自熱水浴取出,靜置自然冷卻至室溫。
(6) 將溶液置於冰水浴,加入10 mL蒸餾水,以玻棒攪拌,使白色沉澱析出,再進行分離及純化。
下列有關此反應的敘述,哪些正確?
(A)乙酐除了作為反應物外,亦可同時作為溶劑,溶解固態的柳酸
(B)步驟(3)加入濃硫酸的目的是為了移除反應所生成的水
(C)步驟(4)的熱水浴是為了加速反應進行
(D)步驟(6)表示阿司匹靈在低溫有較大的溶解度
(E)將氯化鐵溶液加入產物的酒精溶液,若產生紫色,表示產物中有柳酸殘留
113分科化學考科-18
造成臭氧層破壞的可能化學反應,主要來自下列兩個步驟:
步驟一:O₃ + Cl → O₂ + ClO (慢)
步驟二:ClO + O → Cl + O₂ (快)
若此反應的速率定律可表示為 r = k[O₃][Cl],則下列有關臭氧分解的相關敘述,哪些正確?
(A) Cl 是反應的催化劑
(B) ClO 是反應的中間產物
(C) O₂ 是反應的中間產物
(D) 反應的速率決定於步驟一
(E) 反應的速率決定於步驟二
114分科化學考科-12
12. 某反應是一種振盪反應,反應溶液初始為紅色,經過一段時間後轉變為藍色,然後再轉變成紅色。溶液顏色就在紅與藍之間振盪,推測的反應步驟如下:
步驟甲:BrO₃⁻ + 2 Br⁻ + 3 CH₂(COOH)₂ + 3 H⁺ → 3 BrCH(COOH)₂ + 3 H₂O
步驟乙:BrO₃⁻ + 4 Fe(o-phen)₃²⁺ + 5 H⁺ ↔ HOBr + 4 Fe(o-phen)₃³⁺ + 2 H₂O(紅色) (藍色)
步驟丙:HOBr + 2 CH₂(COOH)₂ + 2 Fe(o-phen)₃³⁺ + BrCH(COOH)₂ + 2 H₂O ↔ 2 Fe(o-phen)₃²⁺ + 3 HOCH(COOH)₂ + 2 Br⁻ + 4H⁺
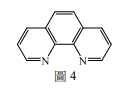
步驟甲中的溴離子濃度降低後,反應則切換至步驟乙,溶液顏色從紅色轉變為藍色。然後步驟丙中錯合物Fe(o-phen)₃³⁺與次溴酸及溴化丙二酸反應後,再生成溴離子,溶液顏色從藍色轉變成紅色。化學式中o-phen的結構如圖所示,為一雙牙基的配位子。下列關於此振盪反應的敘述,哪些正確?
(A)步驟甲中,溴酸根是還原劑
(B)Fe(o-phen)₃³⁺氧化後呈現紅色
(C)步驟乙中,溴酸根產生次溴酸是還原反應
(D)Fe(o-phen)₃²⁺中鐵離子的配位數是6
(E)步驟丙中溶液顏色變化是因為溴離子所造成
114分科化學考科-14
[題組:第14-15題]某生在恆溫下進行 \( Na_2S_2O_3 \) 水溶液的分解反應速率實驗,反應式如下所示:
\[S_2O_3^{2-}+2H^+\rightarrow SO_2+S+H_2O\]
其實驗步驟如下:
(1) 在一個維形瓶中置入 50 mL 的 0.20 M \( Na_2S_2O_3 \) 溶液
(2) 在瓶子底部下方放置一張畫有黑色「X」標誌的白紙
(3) 將 10 mL 的 0.10 M HCl 溶液加入上述維形瓶中,並立刻按下秒錶且以玻棒攪拌
(4) 由維形瓶開口向下觀察,當無法看見白紙上「X」標誌時,停止計時並記錄時間 (t)
(5) 改變步驟(1)的 \( Na_2S_2O_3 \) 溶液體積,並另加入適量蒸餾水。再重複上述步驟進行實驗,結果如表所示。
| Na₂S₂O₃溶液體積(mL) | 蒸餾水體積(mL) | 標誌消失時間t(秒) | 1/t數值(1/秒) |
|---|---|---|---|
| 50.0 | 0 | 33.8 | 0.0296 |
| 30.0 | 20.0 | 49.2 | 0.0203 |
| 10.0 | 40.0 | 150 | 0.0067 |
14. 關於反應式的反應與實驗設計,下列敘述哪些正確?
(A)H⁺是催化劑
(B)是一個氧化還原反應
(C)三個實驗中,加入H⁺的濃度與體積為一定值
(D)可以用Na2S2O3 濃度對t 作圖,得知其為線性關係
(E)若使用20.0 mL Na2S2O3 溶液再進行一次實驗,需使用30.0 mL 蒸餾水
(A)錯誤,H⁺是反應物,非催化劑。
(B)正確,S₂O₃²⁻中S平均氧化數為+2,產物S為0,SO₂中S為+4,有氧化數變化。
(C)正確,每次實驗加入的HCl體積與濃度固定。
(D)錯誤,[Na₂S₂O₃]對t作圖非線性;對1/t作圖接近線性,表示反應速率與[Na₂S₂O₃]成正比。
(E)正確,總體積固定為60 mL,故20 mL Na₂S₂O₃需加40 mL水?(原表總體積為60 mL? 50+10=60, 30+20+10=60, 10+40+10=60,若用20 mL Na₂S₂O₃,則需加蒸餾水60-20-10=30 mL)。答案:BCE
114學測自然考科35
[題組:第35題到第36題]
氧化亞銅為一種半導體材料,其奈米粒子會懸浮在水中,表面可以吸收光能,將二氧化碳轉化成甲醇(CH\(_3\)OH)與氧氣,但氧化亞銅奈米粒子並不會被消耗。持續通入二氧化碳於含氧化亞銅的水溶液中使反應進行,發現光照期間,可觀察到氧氣生成;若將光源關閉,則沒有氧氣生成。
關於實驗結果與推論的敘述,下列哪些正確?(應選3項)
(A)二氧化碳進行還原作用產生甲醇
(B)含有二氧化碳的水溶液呈鹼性
(C)光照是產生甲醇的必要條件
(D)此反應所產生的甲醇與氧氣均離溶於水中
(E)此光照反應式為:2CO\(_2\) + 4H\(_2\)O → 2CH\(_3\)OH + 3O\(_2\)
111學測自然科試題_18
2021年諾貝爾化學獎頒給研究催化劑的學者。人體中的酵素(或稱酶),即是生化反應的催化劑,如胃液中的胃蛋白酶可將蛋白質分解為小的分子片段。酵素的催化能力受環境的溫度、酸鹼性、受質濃度和專一性等影響。下列敘述哪些正確?(應選2項)
(A)酵素通常是胺基酸的聚合物
(B)胃蛋白酶在pH=7.4的環境有最佳活性
(C)溫度越高時,胃蛋白酶的催化能力越強
(D)食用大量制酸劑會降低胃蛋白酶的催化能力
(E)胃蛋白酶亦可將澱粉分解產生葡萄糖